环境化学与生态毒理学国家重点实验室刘思金研究员研究组在大气细颗粒物诱发肺内免疫应答及肺外组织分布方面取得新进展,相关成果以“Lung megakaryocytes engulf inhaled airborne particles to promote intrapulmonary inflammation and extrapulmonary distribution”为题,在线发表于Nature Communications(DOI:10.1038/s41467-024-51686-y)。
大气细颗粒物能否以及如何进入血液循环并扩散至肺外远端器官,是认识细颗粒诱发多组织器官损伤风险中的关键科学问题。环境流行病学和毒理学证据显示,吸入大气细颗粒改变肺内免疫细胞的类群及应答状态,引起肺部及周身炎症,目前细颗粒突破肺屏障实现在肺外器官中再分布的载体和途径尚不清楚。
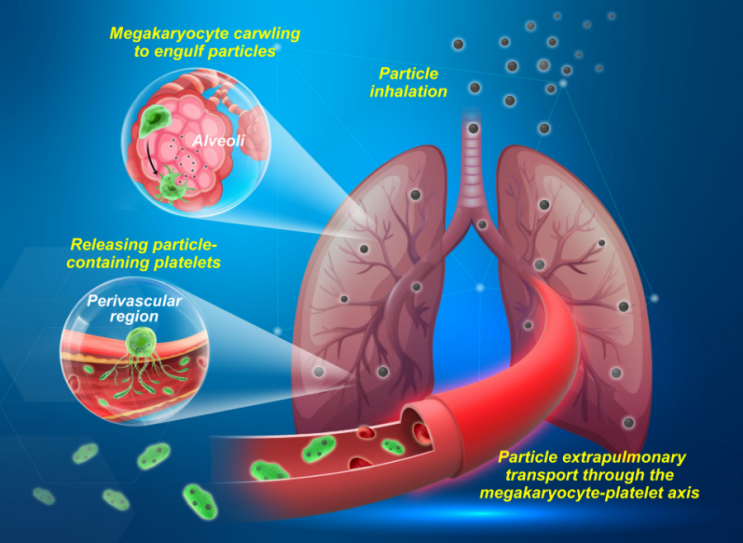
研究团队利用小动物呼吸暴露实验仓,模拟人体呼吸暴露大气细颗粒的剂量,设置不同时长的实验小鼠暴露组。利用多种体内高分辨成像技术,在暴露小鼠肺部识别并鉴定了一种新的肺内原位免疫亚群细胞——肺泡巨核细胞。进一步构建荧光报告基因小鼠,以及对细胞及荧光标记颗粒的体内双示踪模型,发现该细胞能快速捕获并定植颗粒在肺泡内壁,持续刺激肺泡,诱发免疫损伤,在细颗粒暴露诱发的肺损伤中起到关键作用。机制研究表明,肺泡巨核细胞沿肺泡内部爬行“巡逻”,持续捕获入肺的细颗粒,导致细颗粒在细胞膜界面富集,诱发巨核细胞表达多种炎性因子,参与诱发肺内的炎性风暴。更为重要的,巨核细胞是典型的造血细胞,肺泡巨核细胞在吞噬颗粒物后被高度活化并迁移至肺泡毛细血管处,将伪足伸入血管中,在血流剪切力作用下以胞质分裂的方式释放新生血小板进入外周血。新生血小板不仅继承了母源巨核细胞胞内的颗粒,还获得了带有巨核细胞免疫活化分子的细胞膜,一方面使得外周血中具有高粘附与凝血能力的血小板数量增多,增加了肺部及外周器官产生血栓的风险,另一方面血小板作为细颗粒的载体,携载细颗粒随血液循环到达多个肺外器官。
这一研究工作不仅发现了新的、特异性指示细颗粒暴露的新免疫细胞——肺泡巨核细胞,还发现了区别于传统认知中细颗粒直接突破气血屏障的方式,即由细胞携载细颗粒由肺内向肺外传递的细颗粒体内转运新途径。
该文的通讯作者为马娟副研究员,第一作者为2023届博士生丘嘉煌。该研究工作得到国家自然科学基金原始创新项目、国家重点研发计划、中科院青年创新促进会等项目的支持。
论文链接:https://www.nature.com/articles/s41467-024-51686-y?utm_source=rct_congratemailt
&utm_medium=email&utm_campaign=oa_20240827&utm_content=10.1038/s41467-024-51686-y
